PHẦN I MỞ ĐẦU
I. Đặt vấn đề
Hiện nay, vấn đề ô nhiễm Asen và những ảnh hưởng tới sức khoẻ cộng đồng đã được nhiều nước và tổ chức quốc tế quan tâm nghiên cứu. Tại nhiều quốc gia như Bangladesh, Đài loan, Trung Quốc, Ấn độ. Mông Cổ và gần đây là Campuchia đã phát hiện thấy Asen với nồng độ cao ảnh hưởng tới sức khoẻ cộng đồng.
Tại Việt Nam, những nghiên cứu về Asen trong nước ngầm đã được nghiên cứu từ lâu, tuy nhiên vào thời điểm trước đây số lượng mẫu còn ít, mức độ ô nhiễm chưa cao nên vấn đề Asen chưa được quan tâm. Gần đây, với sự hợp tác của các tổ chức quốc tế, các cơ quan nghiên cứu đã tiến hành điều tra khảo sát sơ bộ về tình hình ô nhiễm Asen trong nước ngầm. Kết quả nghiên cứu bước đầu cho thấy hàm lượng Asen trong nước ngầm tại nhiều địa phương (Hà Nam, Hà Tây, Hà Nội, Hưng Yên, Phú Thọ, An Giang, Đồng Tháp,….) cao vượt tiêu chuẩn cho phép.
Theo tổ chức Quỹ nhi đồng liên hợp quốc UNICEF, ô nhiễm Asen ở khu vực phía nam Hà Nội đang là vấn đề nghiêm trọng nhất đối với ô nhiễm Asen ở Việt Nam. Hiện nay, toàn bộ nước sinh hoạt của Hà Nội lấy từ nước ngầm, song tỷ lệ người dân chưa được dùng nước sạch từ các nhà máy nước sạch vẫn còn nhiều. Điều đáng lo ngại nhất là những hộ gia đình sử dụng giếng khoan qua hệ thống xử lý đơn giản hoặc không qua xử lý có nguy cơ rất nhiễm độc Asen rất cao (Qua nghiên cứu 500 giếng khoan vào mùa khố tại một số khu vực như Quỳnh Lôi – HBT, Viện KHCNMT Liên bang Thuỵ Sỹ và liên đoàn địa chất thuỷ văn-công trình miền Bắc cho thấy 34% số điểm mẫu vượt quá hàm lượng cho phép).
Ô nhiễm Asen hiện nay đang là vấn để nhức nhối đối không chỉ ở Hà Nội mà còn nhiều vùng trên khắp cả nước. Chính vì vậy, việc nghiên cứu và tìm ra giải pháp xử lý Asen trong nước ngầm phù hợp cho từng vùng, địa phương là điều hết sức cần thiết.
Trên cơ sở nghiên cứu, phân tích các phương pháp, công nghệ xử lý Asen trong nước ngầm và đánh giá hiện trạng ô nhiễm Asen khu vực Hà Nội, nhóm thực hiện chuyên đề lựa chọn, đề xuất công nghệ xử lý Asen trong nước ngầm quy mô nhỏ, hộ gia đình cho vùng ngoại thành, nông thôn khu vực Hà Nội.
II. Nội dung và phương pháp nghiên cứu:
– Phương pháp điều tra tổng hợp
– Phương pháp kế thừa
– Phương pháp chuyên gia
– Phương pháp phân tích thống kê
– Phương pháp so sánh
PHẦN II NỘI DUNG
CHƯƠNG I. TỔNG QUAN VỀ ASEN VÀ ẢNH HƯỞNG CỦA Ô NHIỄM ASEN ĐỐI VỚI SỨC KHOẺ CON NGƯỜI
1.1. Giới thiệu chung về Asen.
1.1.1. Nguồn gốc và sự tồn tại của Asen trong môi trường.
Asen là nguyên tố khá phổ biến trên trái đất. Trữ lượng asen trong lớp vỏ trái đất khoảng 0,001%, tồn tại chủ yếu dưới dạng các loại quặng như : quặng asenit của Cu, Pb, Ag hoặc quặng sunfua : As2S2; As2S; As2S3,… Asen cũng có thể có trong than đá với hàm lượng cao. Trong khí quyển tồn tại cả asen vô cơ và hữu cơ, người ta phát hiên được sự có mặt của asen trong nước mưa dưới dạng asenit. Ngoài ra asen còn tồn tại trong cơ thể động thực vật. Dưới tác động của các quá trình tự nhiên và nhân sinh khác nhau Asen có thể di chuyển từ các hợp phần môi trường này sang hợp phần môi trường khác dẫn đến sự phân bố phức tạp của các nguyên tố trong tự nhiên.
A – Asen nguồn gốc tự nhiên:
Asen có ở khắp nơi, trong đất đá, nước, không khí và sinh khối. Phần asen chính nằm trong đất đá.
Hình 1.3- Chu trình asen trong tự nhiên
a.1) Asen trong đá và quặng
Hàm lượng As trong các đá magma từ 0,5 – 2,8 ppm, các carbonat – 2,0 ppm, đá cát kết – 1,2 ppm thấp hơn trong các đá trầm tích (6,6 ppm). As là một trong những nguyên tố có nhiều khoáng vật nhất, tới 368 dạng trong đó các nhóm hydroarsen và arsenat – với 213 khoáng vật, sulfurarsenat – 73 khoáng vật, intêmtallit – 40 khoáng vật … Trong các đá phiến sét phần lớn As tồn tại trong silicat (85,5 – 92,5%), phần nhỏ còn lại ở dạng hợp chất khác như oxit, sulfat, arsenua (khoảng 7-14,5 %).
Ở Việt Nam chưa có nhiều nghiên cứu chuyên sâu và toàn diện về As trong các thành tạo tự nhiên. Trước đây, trong công tác lập bản đồ địa chất và tìm kiếm khoáng sản thường dùng phương pháp phân tích qua quang phổ phát xạ với độ nhạy rất thấp nên khó phát hiện As. Bằng phương pháp mầu giã đãi đã tìm thấy trong nhiều phức hệ đá xâm nhập có chứa arsenopyrit với mức hàm lượng As từ <100ppm tới 1000ppm.
Nhìn chung, hàm lượng As trong một số vùng mỏ nguồn gốc nhiệt dịch cao hơn so với khu vực không có khoáng hoá. Có thể có nhiều quặng hoá nguồn gốc nhiệt dịch giàu arsen, hệ số làm giàu của chúng so với đá vây quanh từ hàng chục tới hàng trăm lần và đương nhiên độc tích sinh thái của các quặng này là lớn.
a.2) As trong đất và vỏ phong hoá
Ở nước ta rất ít tài liệu về địa hoá As trong đất. Một số nghiên cứu gần đây về sự phân bố As trong đất vỏ phong hoá ở Việt Nam cho thấy: hàm lượng trung bình của As trong đất Tây Bắc dao động khoảng 2,6 – 11 ppm.
As có xu hướng được tích tụ trong quá trình phong hoá. Trong nhiều kiểu đất ở các cảnh quan địa hoá khác nhau có hàm lượng As giàu hơn đá mẹ. Chẳng hạn, hàm lượng trung bình của As trong các đá trầm tích lục nguyên thuộc mỏ vàng Khau Âu ( Bắc Kạn) là 13 ppm còn trong đất và vỏ phong hoá phát triển trên chúng là 16,9 ppm, đất trong các dị thường quặng tới 92,3 ppm.
a.3) As trong trầm tích bở rời
Hàm lượng tổng As trong bùn biển đại dương thế giới là 1 ppm (A.P Vinogradov, 1967), trong trầm tích Đệ tứ hạt mịn ở Kyoto, Sendai (Nhật Bản) khoảng 1-30ppm. Hàm lượng As trong trầm tích Đệ tứ ở các lỗ khoan nước Hà Nội (6-63 ppm trong trầm tích sét nâu, 2-12 ppm trong sét màu xám 0,5 – 5 trong cát vàng – nâu xám) có quan hệ tuyến tính với hàm lượng Fe(OH)3, FeOOH. Trong trầm tích biển ven bờ Việt Nam có hàm lượng As ( trao đổi ion) dao động trong khoảng 0,1-6,1 ppm.
a.4) As trong không khí và nước
Hàm lượng As trong không khí (ng/m3) của thế giới khoảng 0,007- 2,3 (trung bình 0,5). Hàm lượng As trong không khí ở khu vực xung quanh Ngã Tư Sở là 0,036- 0,071 (trung bình 0,044).
Hàm lượng As trong nước dưới đất phụ thuộc rất nhiều vào tính chất và trạng thái môi trường địa hoá. Dạng As tồn tại chủ yếu trong nước dưới đất là H3AsO¬4-1 (trong môi trường pH axit đến gần trung tính), HAsO4-2 ( trong môi trường kiềm). Hàm lượng As trong nước ngầm trong một số vùng Miền Bắc khoảng 0,0001 – 0,32 mg/l. ở Hà Nội, hàm lượng As trong nước ngầm ở những vùng có trầm tích Đệ tứ với các lớp bùn giàu vật liệu hữu cơ thường cao hơn các vùng khác.
a.5) As trong sinh vật
Theo kết quả nghiên cứu của các nhà khoa học trên thế giới, cây trồng cũng chứa một hàm lượng As nhất định, đôi khi khá cao. Hàm lượng trung bình của As (ppm) trong lúa (khô) 110-200, ngô (khô) 30-40, bắp cải (tươi) 20-50… As tích tụ chủ yếu ở rễ, ở những khu vực đất bị ô nhiễm thì rễ cây hấp thụ khá nhiều As. Hàm lượng As trong rau trước đây (0,1-2,7 ppm trung bình 0,03-0,05 ppm), thấp hơn hàm lượng chính nó trong rau hiện nay. Phải chăng đây là hậu quả của sự ô nhiễm môi trường đất, nước bởi As hiện nay. Sinh vật biển nói chung thường giàu As, hàm lượng trung bình của As trong cá biển từ 0,6-4,7 ppm, còn trong nước ngọt là 0,54 ppm. As tập trung trong gan và mỡ cá.
B – Asen nguồn gốc nhân tạo
Từ các hoạt động của con người asen được phát thải vào môi trường khí, nước, đất. Những nguồn phát thải chính là các hoá chất bảo quản gỗ, công nghiệp, khai khoáng và luyện kim.
b.1) Chất bảo quản gỗ
Ở Mĩ khoảng 90% asen được dùng để chế tạo chất bảo quản gỗ dưới dạng hợp chất asenat đồng crom hoá (CCA). Các thành phần chính của CCA là asen, đồng và crôm. Hoạt chất trong CCA có thể là axit asenic (H3AsO4), asen pentoxit (As2O5) và natri hyđrôasenat (Na2HAsO4).
b.2) Các hoá chất sử dụng trong nông nghiệp
Chủ yếu các hợp chất asen được sử dụng làm chất diệt cỏ, diệt côn trùng, trừ sâu hại, làm rụng lá cây, làm sạch đất. Trong chăn nuôi chúng được sử dụng như những chất phụ gia tăng trọng và ngăn ngừa bện tật trong thức ăn gia súc.
b.3) Các hoá chất sử dụng trong công nghiệp
Asen và hợp chất asen sử dụng khá phổ biến trong công nghiệp. Asen kim loại dùng chế tạo acquy chì-axit, dùng nấu một số hợp kim đồng. Gần đây lượng asen dùng sản xuất acquy chì giảm nhưng asen lại được sử dụng để chế tạo bán dẫn thế hệ mới là AsGa.
Nguồn phát thải quan trong nữa là các quá trình đốt nhiên liệu, sản xuất bột giấy, sản xuất xi măng, sản xuất thuỷ tinh. Các nhà máy đốt than cũng phát thải nhiều asen trong xỉ, bụi tro bay.
Một nguồn phát thải lớn là các lò luyện kim, nơi mà các khoáng chất chứa asen như arsenopyrite, lollingite … được xử lí ở nhiệt độ cao tới 650-700 oC để sản xuất kim loại, hợp kim và các sản phẩm khác nhau. Khói bụi chứa asen không chỉ từ quặng asen mà còn từ chính một lượng than lớn bị đốt cháy.
1.1.2. Cơ chế xâm nhập Asen vào nguồn nước ngầm.
Hiện tượng ô nhiễm asen trong nước ngầm chủ yếu là do hiện tượng giải phóng asen có trong khoáng vật dưới lòng đất. Các nhà khoa học cho rằng asen giải phóng ra nước ngầm theo ba cơ chế sau:
– Cơ chế 1: asen được giải phóng ra bởi sự oxi hoá arsenical pyrite là một khoáng vật phổ biến trong trầm tích, khi mà mực nước ngầm cho phép oxi khí quyển lan toả trong tầng ngập nước.
– Cơ chế 2: anion asen hấp phụ trên khoáng vật ngập nước được giải phóng ra nước bởi sự trao đổi cạnh tranh của anion photphat có mặt do sử dụng của phân bón hoá học.
– Cơ chế 3: dưới điều kiện yếm khí cho phép quá trình khử của sắt oxi hydroxit (FeOOH) và giải phóng asen đã hấp phu trên đó ra nước
1.2. Độc tính của Asen.
1.2.1. Độc tính và cơ chế gây độc của Asen.
Asen ở nồng độ thấp có tác dụng như là một chất kích thích sinh trưởng, nhưng ở nồng độ cao, asen gây độc cho người, động vật. Nếu bị nhiễm độc cấp tính asen có thể gây tử vong trong vài giờ đến một ngày. Trong điều kiện tiếp xúc thường xuyên với asen ở nồng độ vượt quá giới hạn an toàn nhưng chưa gây độc cấp tính, asen gây nhiễm độc mãn tính và thường có biểu hiện với các triệu chứng lâm sàng như: mệt mỏi, chán ăn, giảm khối lượng, xuất hiện các bệnh dạ dày, ngoài da (hội chứng đen da, ung thư da), gan bàn chân, rối loạn chức năng gan.
Qua các thử nghiệm với động vật, các nhà khoa học đã tìm ra giới hạn gây tử vong với một số loài khác nhau là từ 11150 mg/ kg khối lượng cơ thể. Đối với người, liều gây tử vong là: 70 180 mg/ kg khối lượng, kết quả này được rút ra qua những trường hợp bị ngộ độc asen và đã tử vong trong các bệnh viện
Asen đi vào cơ thể bằng tất cả các con đường như: hít thở, ăn uống và thẩm thấu qua da. Trong đó đặc biệt uống nước nhiễm asen là con đường chính để asen xâm nhập vào cơ thể. Khi vào trong cơ thể, đặc biệt là asen (III) tấn công ngay lập tức vào các enzim có chứa nhóm – SH và cản trở hoạt động của chúng. Phản ứng như sau:
asenat cũng giống như photphat, dễ kết tủa với các kim loại và ít độc hơn so với dạng asenit. Khi vào cơ thể asenat thế chỗ của phốtphát trong chuỗi phản ứng tạo adenozintriphotphat (ATP) do đó ATP sẽ không được hình thành :
Khi có mặt asenat, nó sẽ thay chỗ phốt phát:
1.2.2. Biện pháp phòng ngừa.
Nguyên tắc của việc phòng tránh của sự nhiễm độc các tác nhân gây độc cũng như asen là không cho chúng xâm nhập vào cơ thể, khi phát hiện nhiễm độc thì nhanh chóng, kịp thời, chính xác cách ly nạn nhân khỏi nguồn gây độc và giải độc.
Nước uống là nguồn chủ yếu gây nhiễm độc asen. Vì vậy, điều trước tiên cần phải làm là cung cấp nước uống có chất lượng tốt hơn (nồng độ asen đạt tiêu chuẩn cho phép). Điều này chỉ có thể thực hiện được khi chúng ta xử lý tốt nước nhiễm asen hoặc thay đổi nguồn cung cấp.
Khi làm việc với chất có chứa asen cần tránh tiếp xúc với da và mắt, mũi bằng cách sử dụng khẩu trang, kính hay mặt là phòng độc. Không được ăn uống hút thuốc trong quá trình làm việc. Muốn ăn, uống, hút phải rửa tay bằng xà phòng và sau khi làm công việc đã hoàn thành.
Trong trường hợp bị ngộ độc asen, nếu nạn nhân vẫn còn ở trong môi trường nhiễm asen thì ngay lập tức tách nạn nhân ra khỏi đó, cởi bỏ quần áo đã nhiễm asen, rửa sạch người bằng nước sạch, xà phòng; nếu bị vào mắt cần rửa sạch mắt bằng nước sạch ít nhất trong vòng 15 phút. Nếu bệnh nhân vẫn còn tỉnh táo thì cho uống hai cốc sữa (nước) hay trứng sống. Nếu có thể chuyển bệnh nhân tới bệnh viện nhanh nhất.
Để giải độc asen ta tiêm (uống) hoá chất có chữa nhóm – SH như: 2,3đimecaptopropanol: HS –CH2- CH(SH) – OH, chất này có khả năng liên kết với AsO33- nên giảm sự liên kết của AsO33- với nhóm – SH của enzim trong cơ thể.
CHƯƠNG II. THỰC TRẠNG Ô NHIỄM ASEN TRONG NƯỚC NGẦM
KHU VỰC HÀ NỘI
2.1 Tình hình ô nhiễm Asen trên thế giới và ở Việt Nam.
2.1.1 Ô nhiễm Asen trên thế giới.
Như đã trình bày từ đầu, nhiễm độc asen đã không còn là vấn đề riêng của một quốc gia nào. Việc sử dụng nước ngầm là nguồn cung cấp cho sinh hoạt phổ biến ở hầu hết các quốc gia. Vì vậy, hiện trạng nước ngầm nhiễm asen là đáng quan tâm. Trên thế giới hiện nay có rất nhiều nước và vùng lãnh thổ sử dụng nước ngầm bị nhiễm asen một cách trầm trọng như: Tây Bengal (ấn Độ), Băngladesh, Đài Loan, Alaska, một số vùng ở Achentina, Canađa, Mỹ.
Qua phân tích cho thấy nồng độ asen nhiều nơi đã vượt quá giới hạn cho phép của WHO (10 g/l). ở Manikaganj, Harirampar, Faridpur, Gopalganj (Bangladesh) có 19 mẫu thì 14 vượt quá tiêu chuẩn cho phép của Bangladesh (50 g/l), riêng vùng Harirampar cả 4 mẫu đều trên 100 g/l . Nồng độ cao của asen có thể tìm thấy lên tới 1000 g/L. Còn ở phía tây nam Đài Loan nồng độ asen trung bình từ 147671 g/L và người dân sử dụng nước ở đây đã bị bệnh đen chân (blackfoot).
Hai khu vực của Achentina là San Antonio delos Codres và Taco Poro, mỗi nơi nồng độ asen khoảng 200 g/L.
Sự nhiễm asen trong nước ngầm ở phía đông sông Hoogky, một nhánh của sông Hằng phía tây Bengal đã được báo cáo từ đầu năm 1978. Nhóm bệnh nhân đầu tiên được phát hiện vào tháng 7/1983. Kể từ đó phạm vi ảnh hưởng và số bệnh nhân mới ngày càng tăng. Khu vực ảnh hưởng rộng 3400 km2, xấp xỉ 30 triệu dân, số người sử dụng nước nhiễm độc asen lên tới 1 triệu người, trong đó hơn 200 000 người đã được xác nhận là có triệu chứng nhiễm độc asen. Đây là vụ nhiễm độc asen lớn nhất trong lịch sử .
Hiện tượng ô nhiễm nguồn nước ngầm cung cấp cho nước uống của hơn 1 triệu giếng ở Bangladesh và tây Bengal với nồng độ asen vượt quá giới hạn 50 g/ L đã gây nguy hiểm cho hơn 20 triệu người sử dụng nguồn nước đó .
2.1.2 Ô nhiễm Asen ở Việt Nam.
Do cấu tạo địa chất, nhiều vùng ở nước ta nước ngầm bị nhiễm Asen. Khoảng 13,5% dân số Việt Nam (10-15 triệu người) đang sử dụng nước ăn từ nước giếng khoan, rất dễ bị nhiễm Asen.
Theo thống kê chưa đầy đủ, cả nước hiện có khoảng hơn 1 triệu giếng khoan, trong đó có nhiều giếng có nồng độ Asen cao hơn từ 20-50 lần nồng độ cho phép (0.01mg/l), ảnh hưởng xấu đến sức khoẻ, tính mạng của cộng đồng.
Tại vùng đồng bằng châu thổ sông Hồng, những vùng bị nhiễm nghiêm trọng nhất là phía nam Hà Nội, Hà Nam, Hà Tây, Hưng Yên, Nam Định, Thái Bình, … ở vùng đồng bằng sông Cửu Long, cũng phát hiện nhiều giếng khoan có nồng độ Asen cao nằm ở Đồng Tháp và An Giang
Sự ô nhiễm Asen ở miền Bắc phổ biến và cao hơn miền Nam. Gần 1/4 số hộ gia đình sử dụng trực tiếp nước ngầm không qua xử lý Hà Nội đã bị nhiễm Asen, tập trung nhiều ở phía Nam Hà Nội.
Theo ước tính của tổ chức UNICEF tại Việt Nam hiện nay, số người có nguy cơ mắc bệnh do tiếp xúc với Asen lên tới 10 triệu. Sự ô nhiễm Asen trong nước ngầm đã ở mức cao và phổ biến ở vùng châu thổ sông Hồng.
2.2 Thực trạng ô nhiễm Asen trong nước ngầm khu vực Hà Nội.
Hiện nay, toàn bộ nước sinh hoạt của Hà Nội lấy từ nước ngầm, song tỷ lệ người dân chưa được dùng nước sạch từ các nhà máy nước sạch vẫn còn nhiều. Điều đáng lo ngại nhất là những hộ gia đình sử dụng giếng khoan qua hệ thống xử lý đơn giản hoặc không qua xử lý có nguy cơ rất nhiễm độc Asen rất cao (Qua nghiên cứu 500 giếng khoan vào mùa khố tại một số khu vực như Quỳnh Lôi – HBT, Viện KHCNMT Liên bang Thuỵ Sỹ và liên đoàn địa chất thuỷ văn-công trình miền Bắc cho thấy 34% số điểm mẫu vượt quá hàm lượng cho phép).
Theo kết quả phân tích của Trung Tâm Hoá Môi Trường và Viện Hoá Công ghiệp thì nồng độ asen trong nước ngầm một số bãi giếng khu vực Hà Nội vượt quá tiêu chuẩn cho phép 10 g/L (Bộ Y Tế công bố năm 2002). Bảng dưới đây là kết quả phân tích nồng độ asen một số bãi giếng khu vực Hà Nội của Trung Tâm Hoá Môi Trường.
Bảng 2.1- Nồng độ Asen trong nước thô ở một số bãi giếng khu vực Hà Nội
Bãi giếng Nồng độ asen tổng số (g/ L)
Nhà máy nước Tháng 5 Tháng 6
Ngô Sĩ Liên 52,78 20,32
Pháp Vân 348,29 303,79
Mai Dịch 48,24 12,17
Hạ Đình 208,72 218,70
Thanh Mai 78,06 31,07
Lương Yên 67,37 55,03
Yên Phụ 404,33 412,32
Ngọc Hà 42,40 44,48
Qua khảo sát thì thấy ở một số nhà máy nước trong khu vực Hà Nội có nồng độ arsen như sau :
Nguyên nhân gây ô nhiễm Asen trong n¬ước ngầm của vùng.
Nước ngầm bị nhiễm Asen có thể bắt nguồn từ nhiều con đường khác nhau, tuy nhiên có hai nguyên chính sau:
Nguyên nhân từ hoạt động của con người :
+ Do nước thải từ các nhà máy xí nghiệp công nghiệp.
+ Do nước thải từ các làng nghề lân cận.
+ Do canh tác nông nghiệp ở các cùng lân cận.
Arsen xâm nhập vào nguồn nước ngầm qua 3 cách :
– Nơi có độ pH cao .
– Nơi có cacbon hữu cơ.
– Nơi có muối sunphat.
CHƯƠNG III. MỘT SỐ BIỆN PHÁP XỬ LÝ ASEN TRONG NƯỚC NGẦM
3.1. Các phương pháp xử lý.
Hiện nay, có rất nhiều phương pháp để xử lý Asen trong đó có những công nghệ truyền thống, ngoài ra một số công nghệ mới hiện nay đã bắt đầu đưa vào nghiên cứu và ứng dụng. Để thuận lợi khi xem xét ta phân loại theo nhóm các quá trình: các công nghệ kết tủa, các công nghệ hấp phụ, trao đổi ion, lọc mà
3.1.1. Phương pháp kết tủa
a, Keo tụ, lọc.
Keo tụ là quá trình sử dụng hoá chất trung hoà điện tích bề mặt của các hạt cặn lơ lửng, giảm thiểu lực đẩy tĩnh điện làm chúng có khả năng hút nhau tạo các hạt lớn hơn có khả năng tách ra khỏi nước bằng các kĩ thuật đơn giản như lắng trọng lực và lọc cát. Đây là kĩ thuật cổ điển phổ biến trong công nghệ xử lí nước mặt.
Các chất keo tụ phổ biến ở VN là: phèn nhôm (Al2(SO4).18H2O), PAC, ở nước ngoài còn hay dùng FeCl3, Fe2(SO4)3, Fe-polyme.
Để quá trình tạo bông cặn xảy ra tốt hơn người ta còn hay dùng các chất trợ keo tụ hay tạo bông. Chúng thường là các polyme vô cơ (cổ điển) và hữu cơ tan tốt trong nuớc. Mạch polyme dài với các nhóm chức phân cực hoặc tích điện có khả năng “khâu” các hạt cặn nhỏ thành những bông cặn lớn làm tăng khả năng lắng lọc.
Trong quá trình keo tụ các hyđroxit kim loại mới hình thành có khả năng hấp phụ một phần các tạp chất có trong nước cả hữu cơ lẫn vô cơ trong đó có cả asen.
Nhà máy áp dụng quá trình này cần có: bể phản ứng trộn nhanh, hệ kiểm soát pH, bể tạo bông, bể lắng, bể lọc, hệ rửa lọc, hệ xử lí bùn. Nếu hàm lượng cặn không cao có thể bỏ qua bể lắng và áp dụng lọc trực tiếp.
Hiệu quả xử lí As:
Với các chất keo tụ thông dụng (muối nhôm, sắt) As(V) tách loại tốt hơn nhiều so với As(III) (Hering, et al., 1996; Edwards, 1994; Shen, 1973; Gulledge & O’Conner, 1973; Sorg & Logsdon, 1978). Nếu phần lớn asen nằm dưới dạng As(III) cần ôxy hoá thành As(V) trước keo tụ
Ảnh hưởng của loại chất keo tụ:
Thực nghiệm cho thấy, với nồng độ đầu As(V) = 50 g/L, trong khoảng pH =5-8:
Với phèn nhôm: hiệu xuất xử lí đạt 90% với liều cao > 30 mg/L.
Với phèn sắt: hiệu xuất xử lí đạt trên 95% với liều 10-50 mg/L (Gulledge & O’Conner, 1973).
Với nồng độ đầu As(V) = 300 g/L (Logsdon et al. (1974)):
Với phèn nhôm: hiệu xuất xử lí đạt 5-15% với liều cao > 30 mg/L.
Với phèn sắt: hiệu xuất xử lí đạt trên 40-60% với liều 10-50 mg/L (Gulledge & O’Conner, 1973).
Với As(III) pH tốt nhất đối với phèn sắt là 5-8,5 và với phèn nhôm là 5-7. Hiệu xuất xử lí As(III) tăng mạnh nếu ôxy hoá bằng 2 mg clo/L, khi đó hiệu suất đạt 95% đối với phèn sắt và 83% đối với phèn nhôm.
Ảnh hưởng liều lượng chất keo tụ:
Nói chung liều cao thì hiệu suất xử lí cao (Cheng, et al., 1994; Edwards, 1994; Gulledge & O’Conner, 1973; Hering et al. (1996)). Với As(III) sự phụ thuộc vào nồng độ là rất mạnh nhưng As(V) phụ thuộc yếu hơn.
Với As(V) liều phèn Fe thấp (<20 mg/L) cũng đủ nhưng Al cần liều cao hơn (40 mg/L) sẽ đạt hiệu suất trên 90% (Edwards (1994)).
Ảnh hưởng pH:
pH tối ưu đối với phèn sắt là 5-8, phèn nhôm là 5-7 (Sorg & Logsdon (1978)).
Khi nồng độ chất keo tụ cao, ở pH=7,6 hoặc thấp hơn cả hai loại muối đều loại As(V) tốt như nhau. Tuy nhiên khi pH > 7,6 thì phèn sắt (10 mg/L) đạt hiệu suất 87% trong khi phèn nhôm (20 mg/L) chỉ đạt 67% (Edwards (1994)).
Đối với As(III) thì phèn sắt tốt hơn nhôm nhiều.
Ảnh hưởng nồng độ As(III)/As(V) ban đầu:
Với As(V) hàm lượng 100-1000 g/L ở pH tối ưu thì 30 mg/L cả phèn nhôm lẫn sắt đều đạt hiệu xuất > 95% (Logsdon et al. (1974)). Trên 1000 g/L thì hiệu suất giảm khi nồng độ đầu tăng.
Với As(III) hàm lượng lớn hơn 100 g/L cả phèn nhôm lẫn sắt ở liều lượng 30 mg/L đều không hạ được xuống dưới 50 g/L.
Trong cả hai trường hợp khi tăng liều lượng phèn tới 60-100 mg/L thì hiệu quả xử lí tăng.
Ảnh hưởng các chất tan vô cơ:
Các chất tan vô cơ có tiềm năng cạnh tranh hấp phụ với các hạt asen.
Khi nồng độ phèn sắt là 4,9 mg/L, ở pH nhỏ hơn 7, khi có mặt các ion cạnh tranh là Ca2+ và SO42- thì ion sulphát giảm mạnh hiệu xuất xử lí As(III) nhưng lại hơi tăng đối với As(V). Khi pH tăng thì hiệu xuất xử lí As(V) tăng khi có mặt Ca (Hering et al. (1996)).
b, Ôxy hoá sắt, Mangan.
Đây là quá trình phổ biến khi xử lí nước ngầm.
Theo (Edwards, 1994) khi xử lí 2 mg Fe/L đạt được 92,5% hiệu xuất xử lí As(V) với nồng độ đầu là 10 g/L. Nếu nồng độ sắt là 1 mg/L cũng đạt được 83% hiệu xuất xử lí As(V) với nồng độ đầu là 22 g/L.
Tuy nhiên trong quá trình ôxy hoá mangan thì hiệu quả kém hơn. Ví dụ, ôxy hoá 3 mg/L mangan khi có mặt 12,5 g/L As(V) chỉ xử lí được 69%.
Ở nước ngoài và một số vùng ở VN người ta sử dụng cát xanh để thực hiện quá trình lọc – ôxy hoá mangan. Cát xanh là một loại khoáng vật có tên là glauconite chứa nhiều sắt, có màu xanh. Khi sử dụng nó phải được hoạt hoá bằng thuốc tím KMnO4, kết quả là sẽ tạo ra lớp phủ bằng MnO2. Hiệu quả xử lí As(III) là do một loạt quá trình: As(III) hấp phụ lên bề mặt ôxit/hyđroxit Mn (vào vị trí –OH hoặc H¬2O), khi đó nó sẽ bị Mn4+ ôxy hoá thành As(V) còn bản thân Mn4+ biến thành Mn3+ rất dễ bị ôxy hoá ngược lại để lặp lại chu trình, hoặc thành Mn2+ tan vào nước. As(V) hình thành có khả năng hấp phụ mạnh hơn nhiều so với As(III) nên bị cát giữ lại. Số liệu của (Subramanian, et al., 1997) cho thấy có sự tương quan giữa lượng sắt có trong nước ban đầu và khả năng xử lí asen. Khi tỷ lệ Fe/As tăng từ 0 đến 20, ở nồng độ As(III) ban đầu là 200 g/L, nồng độ sulphát = 366 mg/L, TDS = 321 mg/L thì hiệu suất xử lí As tăng từ 41 đến hơn 80%.
c, Keo tụ kết hợp lọc micro
Như trên đã nêu As có thể cố định bằng keo tụ, tuy nhiên phèn nhôm kém sắt do bông nhỏ và độ tan cao của hyđroxit nhôm. Nếu dùng lọc micro có thể ngăn chặn sự lọt qua của các hạt nhỏ, ngoài ra cũng xử lí tốt vi khuẩn.
Lọc micro có các ưu thế sau so với lọc cát:
Lọc được vi sinh
Lọc được bông cặn nhỏ nên giảm chi phí hoá chất
Tăng được công suất nhà máy
d, Keo tụ tăng cường
Kĩ thuật này thường được dùng khi cần giảm nồng độ các chất hữu cơ nhằm tránh sự tạo thành các sản phẩm cơ clo khi sát trùng bằng clo, nhưng nó cũng là một giải pháp tốt để xử lí asen.
Khi tăng nồng độ FeCl3 hoặc phèn nhôm lên 10-30 mg/L, giảm pH xuống 5,5 (Cheng et al. (1994)) nhận thấy rằng As(V) xử lí được trên 90% đặc biệt đối với sắt, phèn nhôm kém hơn. Với nồng độ As(V) đầu bằng 5 g/L chỉ cần 10 mg/L FeCl3 (không chỉnh pH) để đạt hiệu suất 96% trong khi phèn nhôm chỉ đạt 90%. Nếu hạ pH thì phèn nhôm tăng hiệu quả. Đối với sắt thì trong khoảng pH = 5,5-7 yếu tố pH ít ảnh hưởng.
3.1.2. Các phương pháp hấp thụ
Hấp phụ là hiện tượng tập trung chất trên bề mặt phân cách pha. Trong một hệ hấp phụ ta có hai đối tượng: chất hấp phụ và chất bị hấp phụ.
Chất hấp phụ thường là các chất rắn như than hoạt tính, các ôxit và hỗn hợp ôxit kim loại, một số loại nhựa v.v… Để có thể là chất hấp phụ tốt chúng phải có những đặc trưng như: diện tích bề mặt riêng, hệ lỗ xốp thích hợp, các nhóm chức bề mặt thích hợp…
Chất bị hấp phụ chính là các chất tan trong khí, hoặc nước. Đối tượng của chúng ta là những chất tan trong nước, chúng có thể có nguồn gốc tự nhiên hay nhân tạo, có thể là vô cơ hay hữu cơ, có thể gây màu, mùi, có thể là chất độc …
Hiện tượng hấp phụ được gây ra bởi các lực hấp phụ có bản chất rất khác nhau, có thể là lực hút tĩnh điện, lực cảm ứng, lực phân tử (lực van der Vaals) …
Các quá trình hấp phụ có thể được thực hiện bằng nhiều cách khác nhau, tuỳ vào cách thực hiện ta có những kĩ thuật cụ thể. Ví dụ, khi chất hấp phụ được sản xuất và áp dụng dưới dạng hạt cỡ mm, ta sử dụng kĩ thuật lọc hấp phụ tương tự như lọc cát; nếu chất hấp phụ dưới dạng bột mịn ta sử dụng kĩ thuật khấy trộn-phản ứng kết hợp lắng như trong đánh phèn thông thường.
a, Ôxit nhôm hoạt tính (AA)
Quá trình hấp phụ ở đây thực chất là trao đổi ion với các nhóm OH bề mặt của nhôm hoạt tính-AA
AA điều chế từ hyđroxit nhôm bằng cách nung ở nhiệt độ nhất định, nó là hỗn hợp -ôxit nhôm và ôxit nhôm vô định hình . Thường được chế tạo dưới dạng viên và sử dụng trong các cột lọc để xử lí flo, selen, silica, hữu cơ và cả asen. Khi hết dung lượng hấp phụ nó có thể tái sinh bằng cách rửa qua dịch kiềm NaOH, trung hoà bằng axit rồi tráng bằng nước sạch trước khi đưa trở lại làm việc.
Các yếu tố ảnh hưởng tới hiệu quả xử lí là pH, dạng asen, các ion cạnh tranh, thời gian tiếp xúc và cách tái sinh.
Ảnh hưởng của pH
pH=8,2 là điểm đẳng điện nghĩa là ở đó AA không tích điện, trên đó sẽ tích điện âm (do hấp phụ OH-) và dưới đó sẽ tích điện dương (do hấp phụ H+). Như vậy đối với các anion, Ví dụ: asenat pH dưới 8,2 sẽ hấp phụ mạnh.
Tuy nhiên vẫn có một số công trình cho rằng pH tối ưu là 5,5-6,0. Kết quả nghiên cứu cho thấy khi hạ pH từ 7,5 tới 6 có thể tăng lượng nước xử lí được từ 2 đến 12 lần. Tương tự khi pH tăng từ 6,0 đến 9,0 thì khả năng hấp phụ As(V) của AA bị mất:
Ảnh hưởng của trạng thái ôxy hoá của As:
As(V) hấp phụ tốt hơn (III). Tại pH6,0 (Frank et al., 1986) đã thử với lọc hai loại asen trong nước thô có cùng nồng độ là 100 g/L. Cột lọc As(V) cho kết quả 23.400 thể tích có nồng độ dưới 50 g/L, trong khi cột lọc As(III) chỉ lọc được 300 thể tích.
Ảnh hưởng của các ion cạnh tranh:
Về nguyên tắc hấp phụ là quá trình cạnh tranh nên các ion đều có tiềm năng ảnh hưởng, tuy nhiên AA tỏ ra là khá ưu tiên As(V). Sau đây là dãy thứ tự hấp phụ ưu tiên trên AA.
OH > H2AsO4 > Si(OH)3O > F > HSeO3 > TOC > SO42 > H3AsO3
Ta thấy sulphát có mặt bên phải As tức là ảnh hưởng rất yếu (Benjamin et al. 1998), H3AsO3 đứng cuối dãy nghĩa là hấp phụ rất yếu. Tuy nhiên chất hữu cơ (TOC) mặc dù xếp sau ảnh hưởng khá: 4 mg/L TOC giảm hiệu quả 50%. Sulphát và các chất tan khác (TDS) nếu cao cũng ảnh hưởng: 360 mg/L sulphát và 1000 mg/L TDS giảm 50% hiệu quả hấp phụ asen bởi AA. Tương tự clorua ở nồng độ cao cũng giảm nhưng không mạnh bằng sulphát.
Ảnh hưởng của thời gian tiếp xúc:
Thí nghiệm với nước hồ Washington (Benjamin et al. 1998) ở pH7,0 với thời gian tiếp xúc tăng dần từ 2,5 tới 15 phút cho thấy 2000 thể tích nước lọc có nồng độ asen < 5 g/L, thời gian tiếp xúc tăng chỉ tăng nhẹ lượng asen bị hấp phụ.
Ảnh hưởng của tái sinh:
Để tái sinh AA cần dung dịch kiềm đặc (NaOH 4%), thể tích dịch tái sinh phải gấp vài lần thể tích vật liệu lọc. Sau kiềm phải trung hoà bằng dịch H2SO4 2%. Sau khi tái sinh AA giảm hiệu quả, đặc biệt sau hai lần tái sinh.
Hiệu ứng thứ cấp:
AA có thể thay đổi tính chất nước. Khi phải hiệu chỉnh pH để đạt pH6 tối ưu nước ra sẽ có pH nhỏ, do đó cần tăng pH để kiểm soát ăn mòn hệ phân phối.
Để đơn giản hoá, đối với các hệ nhỏ đôi khi người ta làm việc ở pH cao. Ví dụ có hai trạm đã làm việc kiểu này được nghiên cứu khi đó thời gian làm việc của cột lọc hấp phụ sẽ ngắn hơn.
Silica, các hạt SS, vi khuẩn có thể gây tắc, cần rửa ngược định kì.
3.1.3. Trao đổi ion
Bản chất là phản ứng trao đổi của các ion trên bề mặt chất rắn (chất trao đổi ion) với các ion cùng dấu trong dung dịch, quá trình này nói chung là thuận nghịch.
Chất trao đổi ion có thể là nhựa, các ôxit hoặc hỗn hợp ôxit tổng hợp hoặc tự nhiên.
Tương tự các kĩ thuật hấp phụ kĩ thuật trao đổi ion thường được thực hiện dưới dạng các cột lọc gọi là cột lọc hoặc trao đổi ion, đôi khi cũng thực hiện trong bồn phản ứng khuấy trộn.
Trong kĩ thuật lọc nước vào có thể đi từ trên xuống hoặc dưới lên qua lớp vật liệu trao đổi ion dạng hạt. Đôi khi để tăng tốc độ và hiệu quả quá trình người ta áp dụng kĩ thuật phản ứng với lớp đệm giả sôi (hoặc lớp đệm lơ lửng hoặc lớp đệm mở rộng), khi đó hạt trao đổi ion phải nhỏ, nước đi từ dưới lên với tốc độ lớn làm các hạt vật liệu như treo trong dòng chất lỏng, tăng khả năng tiếp xúc và vận tốc quá trình tối đa.
Khi vật liệu trao đổi ion bão hoà (hết khả năng trao đổi), ta phải tái sinh. Tái sinh là quá trình ngâm rửa vật liệu trong môi trường dung dịch chứa ion gốc của vật liệu trao đổi, khi đó sẽ xảy ra quá trình trao đổi ngược: ion gốc sẽ thay thế ion vừa bị bắt giữ trên bề mặt vật liệu trao đổi, khi đó trong nhiều trường hợp vật liệu lại khôi phục trạng thái ban đầu (quá trình này còn đồng ngiã với quá trình rửa giải ion bị hấp phụ. Tái sinh cũng là giải pháp bắt buộc khi cột lọc đã lọc đủ số BV đã tính. Trong phần lớn các trường hợp dung dịch tái sinh có dung tích khoảng 1 đến 5 BV. Khi tái sinh xong phải rửa-tráng bằng 2 đến 20 BV nước sạch, trong một số trường hợp để tiết kiệm có thể dùng nước thô.
Những thông số ảnh hưởng nhiều đến hiệu quả quá trình là pH, bản chất và nồng độ các ion, các chất cạnh tranh, loại nhựa (kể cả kích thước), độ kiềm, nồng độ chất cần xử lí, thời gian tiếp xúc.
Trong kĩ thuật lọc thời gian tiếp xúc được tính bằng thời gian nước lưu trong thể tích cột lọc rỗng bằng thể tích mà vật liệu chiếm chỗ. Nó thường được đo bằng phút và tính bằng (t):
t = V/Q
Trong đó: V- thể tích vật liệu (L hoặc m3)
Q- lưu lượng nước xử lí (L hoặc m3/phút)
Trong quá trình lọc trao đổi ion các chất cặn lơ lửng, hữu cơ tan, vi sinh có thể tích luỹ trong cột gây tổn thất áp đáng kể hoặc không đáng kể, dù không vẫn nên định kì rửa ngược bằng nước sạch để ngăn ngừa hiện tượng tích luỹ vi sinh.
Các yếu tố ảnh hưởng tới hiệu quả xử lí:
Ảnh hưởng của pH
Vật liệu trao đổi ion để lọc asen thường là nhựa trao đổi anion tổng hợp chứa ion gốc là Cl-. Chúng hoạt động tốt ở pH =8-9 nếu là nhựa bazơ mạnh, mặc dù vùn pH được xác định cho loại nhựa này là 6,5-9.
Trong xử lí asen, nhựa trao đổi loại bazơ amnhj là thích hợp. So với loại bazơ yếu vùng pH tối ưu của bazơ mạnh rộng hơn nên dễ sử dụng hơn.
Ảnh hưởng của các ion cạnh tranh
Sự hấp phụ cạnh tranh từ phía các ion có trong nước thô sẽ xác định tính kinh tế của quá trình. Nếu cạnh tranh quá mạnh, số BV nước lọc hiệu quả giảm mạnh, tần suất tái sinh tăng làm tăng chi phí vận hành.
Với nhựa bazơ mạnh ta có dãy hấp phụ ưu tiên từ trái sang phải như sau:
HCrO4 > CrO42 > ClO4 > SeO42 > SO42 > Br > HPO42, HAsO42, SeO32, CO32 > NO3 > NO2 > Cl > H2PO4, H2AsO4, HCO3 > OH > CH3COO > F
Nếu chỉ tính những anion phổ biến trong nước ta có dãy rút gọn sau:
SO42 > HPO42, HAsO42 > NO3 > Cl > H2PO4, H2AsO4, HCO3
Như vậy những ion đứng bên trái HAsO42 là các ion cạnh tranh làm giảm hiệu quả hấp phụ đối với asen nhất.
Ảnh hưởng của loại nhựa trao đổi ion
Như đã nêu nhựa loại bazơ mạnh tuy tốt nhưng vẫn ưu tiên sulphát và ở mức độ nhất định clorua. Sự nghiên cứu các loại nhựa chọn lọc theo ion cần xử lí hứa hẹn những ứng dụng tin cậy hơn của phương pháp này.
Danh mục một số loại nhựa trao đổi khá tốt đối với asen được nêu ở bảng 2.1.
Bảng 3.1- Danh mục một số nhựa trao đổi ion dùng để xử lí asenat
Tên nhựa Loại Đặc trưng vận hành Số BV Nguồn
Dowex 11 2 Thể tích nhựa: 0,8 cu ft
Lưu lượng: 1 gpm
t (EBCT): 5,6 min
Chiều cao lớp VL: 2,5 – 5 ft
Tỷ lệ Sulphát/As: 60:1
Tỷ lệ TDS/As: 2500:1 4.200 Clifford & Lin
(1986)
Ionac ASB-2 2 Thể tích nhựa: 0,8 cu ft
Lưu lượng: 1 gpm
t (EBCT): 5,6 min
Chiều cao lớp VL: 2,5 – 5 ft
Tỷ lệ Sulphát/As: 60:1
Tỷ lệ TDS/As: 2500:1 4.940
Dowex SBR-1 1 Thể tích nhựa: 1,0 cu ft
Lưu lượng: 1 gpm
t (EBCT): 7,5 min
Chiều cao lớp VL: 7,5 ft
Tỷ lệ Sulphát/As: Không xác định
Tỷ lệ TDS/As: Không xác định 2.800 Hathaway &
Rubel (1987)
Fox (1989)
Ionac ASB-1
– & –
Dowex 11
1 Thể tích nhựa: 0,014 cu ft
Lưu lượng: Không xác định
t (EBCT): Không xác định
Chiều cao lớp VL: Không xác định
Tỷ lệ Sulphát/As: 420:1
Tỷ lệ TDS/As: 9200:1 200
400-500
[As(III) ôxy hoá thành As(V)] Clifford & Lin
(1985)
A-300E
(bench-scale)
A-300E
(quy mô SX)
2 Thể tích nhựa: 0,0018 cu ft
Lưu lượng: 0,035 gpm
t (EBCT): Không xác định
Chiều cao lớp VL: 1,33 ft
Tỷ lệ Sulphát/As: 300:1
Tỷ lệ TDS/As: Không xác định 1.340-1.640
5.000-7.000 Malcolm Pirnie
(1992)
3.1.4. Các quá trình màng – Membrane
Màng lọc một cách đơn giản có thể xem như một cái rây cơ học nghĩa là nó cho qua những hạt có kích thước nhỏ hơn kích thước của lỗ trống và giữ lại những hạt lớn. Tuy nhiên ở quy mô phân tử và trong môi trường dễ tạo liên kết như môi trường nước nhiều hiệu ứng như hyđrat hoá, tạo phức, polime hoá ít nhiều làm sai lệch khái niệm trên.
Động lực của quá trình lọc màng là sự chênh lệch hoá thế giữa hai phía của màng lọc và áp suất, hoặc chênh lệch điện thế. Các kĩ thuật lọc được phân loại theo kích thước hạt lọc được, bản chất động lực quá trình, hình thái và bản chất màng …
Đối với quá trình mà động lực là áp suất ta có các loại quá trình (theo chiều giảm dần kích thước lỗ): lọc micro (vi lọc-MF); siêu lọc (UF); lọc nanô (NF); lọc RO (thẩm thấu ngược). áp suất áp dụng như sau:
3.1.5. Các kĩ thuật khác
a, Lọc bằng cát phủ ôxit sắt.
Cát lọc phủ ôxit(hyđroxit) sắt có khả năng hấp phụ/trao đổi ion (với nhóm –OH bề mặt) để lọc asen cũng như một số kim loại khác. Tương tự các chất hấp phụ/trao đổi ion khác nó có thể tái sinh (bằng kiềm). Các yếu tố ảnh hưởng tới hiệu quả quá trình là pH, trạng thái của As, sự có mặt của các ion cạnh tranh, tốc độ lọc (thời gian tiếp xúc tính theo thể tích chiếm chỗ vật liệu rỗng), quy trình tái sinh.
Ảnh hưởng của pH
Khi pH tăng từ 5,5 đến 8,5 hiệu quả hấp phụ As(V) giảm khoảng 30% (Benjamin et al. 1998).
ảnh hưởng của trạng thái ôxy hoá của As:
As(V) hấp phụ tốt hơn (III) kể cả về tốc độ lẫn lượng hấp phụ.
Ảnh hưởng của các ion cạnh tranh:
Khi nồng độ sulphat tăng từ 0-100 mg/L ảnh hưởng không đáng kể, ion clo không ảnh hưởng, chất hữu cơ có ảnh hưởng cạnh tranh, DOC = 4 mg/L giảm khả năng hấp phụ As(V) 50% (Benjamin et al. 1998).
Ảnh hưởng của thời gian tiếp xúc:
Thí nghiệm với nước hồ Washington ở pH = 7 (Benjamin et al. 1998) cho thấy khi thời gian tiếp xúc tăng từ 2,5 đến 15 phút As ở nước ra < 5 g/L ổn định sau 2000 giờ lọc.
Thời gian tiếp xúc tăng làm tăng nhẹ hấp phụ. Khả năng hấp phụ đạt 175-200 g As/mL vật liệu lọc.
Ảnh hưởng của tái sinh:
Tái sinh cát phủ ôxit sắt tương tự đối với ôxit nhôm, tức là chất rửa giải là dung dịch NaOH, trung hoà bằng H2SO4. Nếu NaCl 0,1N và NaOH 0,2N không tái sinh tốt, chỉ tái sinh được dưới 50% khả năng hấp phụ ban đầu.
b, Sắt sulphua hoá
Đây là một patent (Hydrometrics, 1997 &1998). Để tạo sắt sulphua hoá cần đi từ bột sắt mịn, bột lưu huỳnh mịn và một chất ôxy hoá (H2O2). Ba tác nhân trên trộn kĩ rồi đưa vào nước cần xử lí. H2O2 dùng để ôxy hoá As(III) thành (V). Tác nhân này thử với nhiều loại nước khác nhau và thu được nồng độ As dưới 50 g/L.
Hiệu quả phụ thuộc vào pH:
Với pH 8: 1 gam sắt xử lí được 20 mg As
Với pH 7: 1 gam sắt xử lí được 50 mg As
Có thể áp dụng kĩ thuật lọc. Với thời gian lưu từ 5 đến 15 phút hiệu quả khá cao, tỷ lệ As/Fe = 11 mg/g.
c, Vật liệu lọc hyđroxit sắt dạng hạt
Đây là vật liệu được đề xuất bởi ĐHTH Berlin (Driehaus et al. 1998). Vật liệu này cho phép lọc được lượng nước bằng 30.000 đến 40.000 thể tích vật liệu với nồng độ As(V) đầu ra không bao giờ vượt quá 10 g/L. Vật liệu lọc có thể thôi ra nước với mức độ 5-25 mg/L có chứa 1-10 g As/kg. Vật liệu có tên GHF.
Bảng 3.2- Kết quả thử vật liệu lọc hyđroxit sắt
Đơn vị TN1 TN2 TN3 TN
Chất lượng nước thô
pH 7,8 7,8 8,2 7,6
Nồng độ asenat g/L 100-800 21 16 15-20
Nồng độ phốt phát g/L 0,70 0,22 0,15 0,30
Độ dẫn S/cm 780 480 200 460
Khả năng hấp phụ asenat g/kg 8,5 4,5 3,2 N/D
Cột hấp phụ
Chiều cao m 0,24 0,16 0,15 0,82
Tốc độ lọc m/h 6-10 7,6 5,7 15
Lượng nước xử lí BV 34.000 37.000 32.000 85.000
Nồng độ asen tối đa trong SP g/L 10 10 10 7
Hàm lượng asen trong GFH g/kg 8,5 1,4 0,8 1,7
Tổn thất GFH (lượng khô) g/m3 20,5 12 18 8,6
Ion sulphat cạnh tranh với As không đáng kể song phốt phát rất mạnh, Sự giảm pH dẫn tới giảm hiệu quả hấp phụ, đây là đặc trưng cho hấp phụ anion,
GFH tốt hơn ôxit nhôm ở pH cao nhưng tương đương ở pH thấp hơn 7,6. So với nhôm hoạt tính (AA) thì nó tái sinh được nhiều lần hơn, năng lực hấp phụ cao hơn AA nên thiết bị nhỏ hơn với cùng nhiệm vụ, đặc biệt nó không cần tiền ôxy hoá?
d, Phoi sắt
Trong kĩ thuật này nước được tưới lên phoi sắt rồi lọc cát, Sắt sẽ hoà tan rồi đồng kết tủa với asen tạo arsenopyrite kết tủa, vì vậy sự có mặt của ion sulphát là cần thiết, Các thử nghiệm cho thấy hiệu xuất xử lí khá cao, đạt 81% với nồng độ asen tới 20.000 g/L, với nồng độ 2000 g/L sản phẩm ổn định có mức asen dưới 50 g/L (nồng độ tối đa cho phép-MCL), Tuy nhiên rất khó áp dụng vì nó đòi hỏi thời gian tiếp xúc tới 7 ngày và cũng chưa có thông tin là nó có thể giảm nồng độ asen xuống dưới 25 g/L,
e, Ôxy hoá quang hoá
Các chuyên gia Tổ chức khoa học và công nghệ hạt nhân úc (ANSTO) phát hiện rằng khi có mặt các tác nhân hấp thụ ánh sáng và có ánh sáng thì As(III) rất dễ bị ôxy hoá bằng ôxy không khí, tốc độ nhân lên hàng chục nghìn lần (Cooperative Research Centres for Waste Management and Pollution Control Limited, 1999), Khi đó As dễ dàng được loại bỏ bằng kĩ thuật đồng kết tủa và lọc, Các thí nghiệm với nước chứa tới 12 mg/L As(III) cho thấy khi có mặt một số kim loại (ví dụ nước mỏ), ở môi trường axit, có tia UV hay ánh sáng mặt trời 97% As(III) biến thành As(V), Đặc biệt tốt khi có nhiều Fe(II) với tỷ lệ mol Fe:As=22:1. Bằng phương pháp này nước khai mỏ có thể dễ dàng đạt được nồng độ asen nhỏ hơn 17 g/L.
3.2. Đề xuất giải pháp trồng cây Dương xỉ để xử lý Asen trong nước ngầm
cho vùng nông thôn khu vực Hà nội.
Như vậy, có rất nhiều giải pháp có thể lựa chọn để xử lý Asen trong nước ngầm, song giải pháp nào là phù hợp thì còn phụ thuộc vào nhiều yếu tố như: điều kiện tự nhiên, kinh tế – xã hội, mức độ xử lý, đặc điểm của nguồn nước,….Sau đây là những đánh giá sơ bộ về những ưu, nhược điểm của từng phương pháp:
– Ph¬ương pháp kết tủa: đòi hỏi mức độ đầu t¬ư và quản lí cao, phù hợp với nhà máy công suất lớn. Hiệu suất xử lí cao, lượng nước tổn thất thấp. Quá trình xử lí cần sử dụng nhiều loại hoá chất, đòi hỏi oxi hoá sơ bộ, điều chỉnh độ pH và xử lí bùn cặn. Việc xử lí bùn cặn khá phức tạp và tốn kém.
– Ph¬ương pháp hấp phụ: không đòi hỏi yêu cầu đầu t¬ư và quản lí cao, phù hợp với nhà máy công suất trung bình và nhỏ. Hiệu suất xử lí t-ương đối cao, l¬ượng n¬ớc tổn thất thấp. Quá trình xử lí cần oxi hoá sơ bộ, điều chỉnh pH và xả cặn. Cột vật liệu hấp thụ cần đ¬ược bổ sung và rửa thư¬ờng xuyên.
– Ph¬ương pháp trao đổi ion yêu cầu mức đầu t¬ và quản lí trung bình, phù hợp với nhà máy công suất nhỏ. Hiệu xuất xử lí t¬ơng đối cao, l-ượng nư¬ớc tổn thất thấp. Quá trình xử lí đòi hỏi oxi hoá sơ bộ và xả cặn nh¬ng không cần điều chỉnh pH. Cột vật liệu trao đổi ion cần đ¬ược bổ sung và rửa thư¬ờng xuyên.
Các ph¬ương pháp trên đều có khả năng xử lí Asen với hiệu quả cao, song yêu cầu về đầu t¬ư lớn và trình độ quản lí cao. Do đó các ph¬ương pháp này thích hợp cho xử lí Asen với quy mô tập trung ở các nhà máy n¬ước.
Đối với quy mô nhỏ, hộ gia đình thì các phương pháp trên rất khó áp dụng triển khai bởi những khó khăn như đã nêu. Hiện nay, một phần không nhỏ các hộ gia đình nông thôn, ngoại thành Hà nội hiện đang khai thác, sử dụng nước ngầm đang tiềm ẩn nguy cơ ô nhiễm Asen trong đó. Đối với những nơi có nguy cơ ô nhiễm Asen cao như ở Hà Nội thì hàm lượng Asen trong nước ngầm không thể lọc hết bởi những thiết bị lắng, lọc đơn giản hoặc còn nguy hiểm hơn nữa khi một bộ phận người dân còn sử dụng trực tiếp nước ngầm mà không qua bước xử lý nào cả. Trong khi đó, xử lí n¬ước ngầm có chứa kim loại nặng cho quy mô hộ gia đình bằng biện pháp sinh học đang là một trong những ¬ưu tiên hàng đầu, do những biện pháp hóa lí tỏ ra chậm, tốn kém và phức tạp. Các ¬ưu điểm công nghệ sinh học các ¬ưu điểm là không gây ô nhiễm môi trường, rẻ tiền và dễ tiến hành, triển khai trên diện rộng.
Giải pháp sử dụng cây Dương xỉ, một loại cây mọc dại phổ biến ở Việt Nam, gần đây đã được các nhà khoa học Trung Quốc, Mỹ,…và Việt Nam nghiên cứu như một loại thực vật có khả năng siêu hấp thụ Asen (Mỗi kg thực vật có khả năng hấp thụ 22 gram Asen – Theo Nature ).
Cây Dương xỉ có tên khoa học là Pteris vittata mọc dại rất nhiều ở Việt Nam, phát triển nhanh trong điều kiện khí hậu nóng ẩm. Những ưu việt của loài cây Dương xỉ khi áp dụng để hấp thụ Asen trong nước ngầm đó là:
Sinh khối lớn và luôn tăng.
Hệ thống rễ trải rộng.
Khả năng hấp thụ Asen lớn và nhanh chóng.
Sức sống mạnh
Sau đây là một số những kết quả nghiên cứu về khả năng xử lý ô nhiễm Asen của cây Dương xỉ.
Những yếu tố ảnh hưởng đến hiệu suất xử lý:
– Hoá trị của Asen: Cây có khả năng hấp thụ cả As(III) và As(V) nh¬ưng hiệu quả hơn với As(V).
– Tuổi cây: Sử dụng cây ít tuổi hiệu quả hơn so với cây nhiều tuổi.
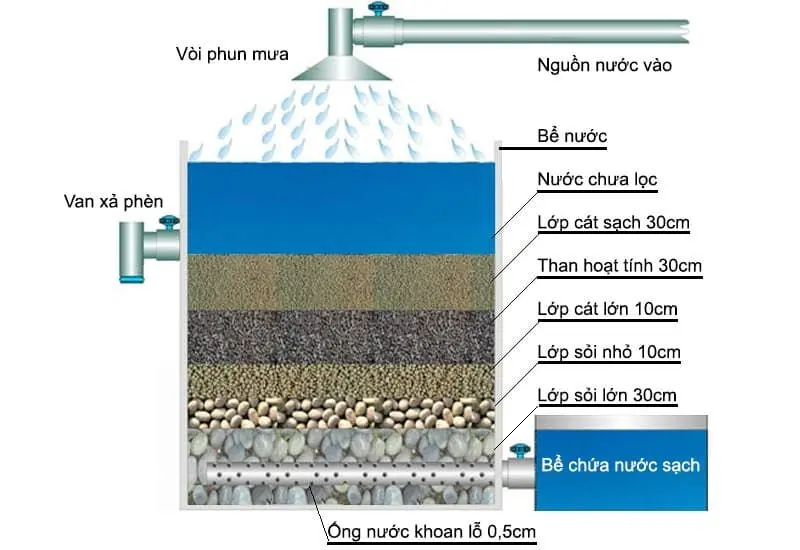
Đề xuất dây chuyền công nghệ xử lý ô nhiễm Asen trong nước ngầm quy mô hộ gia đình cho vùng ngoại thành, nông thôn khu vực Hà Nội:
PHẦN III KẾT LUẬN VÀ ĐỀ XUẤT Ý KIẾN
I. Kết luận
Ô nhiễm Asen trong nước ngầm khu vực Hà Nội đã đến mức báo động nghiêm trọng đặc biệt là khu vực phía nam Hà Nội. Nhiều giếng khoan nước ngầm mạch nông ở khu vực này bị ô nhiễm Asen cao vượt nhiều lần so với tiêu chuẩn cho phép.
Các ph¬ương pháp hoá lí: yêu cầu về vốn, kĩ thuật và quản lí cao nên áp dụng cho xử lí tập trung tại các nhà máy n¬ước có quy mô vừa và lớn.
Giải pháp sử dụng trồng cây Dương xỉ để xử lý ô nhiễm Asen trong nước ngầm cho vùng nông thôn, ngoại thành khu vực Hà Nội có nhiều ưu điểm: Đơn giản, hiệu quả, rẻ tiền và dễ áp dụng trên diện rộng.
II. Đề xuất ý kiến
Qua nghiên cứu, tìm hiểu về nguồn gốc hình thành và độc tính của Asen nói chung cũng như ở khu vực Hà Nội nói riêng, nhóm chuyên đề xin đưa ra một số ý kiến như sau:
Khẩn trương lập báo cáo điều tra, đánh giá hiện trạng ô nhiễm Asen trong nước ngầm trên phạm vi toàn Hà Nội nhằm phục vụ cho công tác quản lý cũng như triển khai các chương trình ngăn chặn, khắc phục ô nhiễm Asen trong tương lai.
Sử dụng các giải pháp chi phí thấp, bền vững và có khả năng áp dụng rộng rãi trong cộng đồng phải được xem như là giải pháp tiếp cận cần ưu tiên. Đó cũng chính là phương thức tiếp cận lấy con người và chất lượng cuộc sống của họ làm trung tâm.
Kết hợp các giải pháp “cứng”: đầu tư xây dựng cơ sở vật chất với các giải pháp “mềm”: nâng cao nhận thức cộng đồng. Vấn đề nâng cao nhận thức cộng đồng cần đi trước.
TÀI LIỆU THAM KHẢO
1. PGS-TS. Trần Đức Hạ – Đỗ Văn Hải – Cơ sở của quá trình xử lý nước cấp và nước thải – NXB Khoa học và kỹ thuật năm 2002.
2. PGS. TS Cao Thế Hà, TS. Nguyễn Hoài Châu – Công nghệ Xủ lý nước nguyên lý và thực tiễn – NXB Thanh Niên năm 1999.
3. GS. TS Trần Hiếu Nhuệ – Cấp nước và vệ sinh nông thôn – NXB Khoa học và kỹ thuật năm 2002.
4. Đỗ Văn Ái, Mai Trọng Nhuận – Một số đặc điểm phân bố Asen trong tự nhiên và vấn đề ô nhiễm Asen ở Việt Nam – Viện Địa chất và Môi trường, Đại học Khoa Học Tự Nhiên, Đại học Quốc gia Hà Nội.
5. Tiêu chuẩn TCXD 33 – 2006 “Cấp nước – Mạng lưới đường ống và công trình – Tiêu chuẩn thiết kế”
KS. Vũ Thị Hoài Ân